Syndrom akrální mutilace (AMS) je dědičné onemocnění nervového systému, vyskytující se u několika plemen psů. Nejvýznamnějším pozorovatelným příznakem je lízání až kousání tlapek. Projevuje se nejčastěji mezi 2. a 12. měsícem života. Onemocnění není léčitelné.
Pokud jste někdy viděli svého psa olizovat si tlapky, patrně jste si řekli, že se pouze čistí, nebo se jenom nudí, případně ho něco svrbí, ale brzy to přejde. S nejvyšší pravděpodobností máte pravdu a může se jednat o jakýkoliv méně závažný problém. Často se takto projevuje například alergie na krmivo a po vyřazení nevhodné složky potravy se vše vrátí do starých kolejí. Ovšem, pokud vám právě u nohou leží příslušník některého z plemen ohařů či španělů měli byste zbystřit, protože tento text pojednává o velice nepříjemném onemocnění, které se vyskytuje zrovna u těchto plemen.
Syndrom akrální mutilace (anglicky: acral mutilation syndrome – AMS) je onemocnění řadící se mezi dědičné motorické a senzorické neuropatie. Pod označením „Nekróza prstů ohařů“ jej poprvé v roce 1964 popsal český veterinář MVDr. Ladislav Pivník u německých krátkosrstých ohařů. Následně bylo velice podobné onemocnění zjištěno u anglických pointerů v Severní Americe, u anglických špringršpanělů v Austrálii a u francouzských dlouhosrstých ohařů v Kanadě. Ve všech případech se předpokládá stejná příčina. AMS bylo popsáno, také u fenky miniaturního pinče, nicméně v tomto případě není jisté, zda se nejednalo pouze o náhodnou mutaci.1,2,3,4
Příčina a rozvoj nemoci
Za vznikem onemocnění stojí bodová mutace v lincRNA (long intergenic non-coding RNA), což jsou úseky genomu, které plní různé regulační funkce. Tato mutace se nachází v blízkosti genu GDNF (glial cell-derived neurotrophic factor), jež je předlohou specifického proteinu odpovědného za správný vývoj a životnost neuronů. Tato mutace tak narušuje podporu exprese genu, což má za následek špatný rozvoj senzorických nervových vláken a jejich postupnou degeneraci až zánik. Nedochází však k úplné zástavě exprese, a patrně proto není tato mutace letální. Postižená jsou pouze senzorická nervová vlákna, nikoliv motorická a autonomní nervový systém. Dochází k poruše zpracování a přenosu bolestivých vjemů (nocicepce), snižuje se citlivost na horko, chlad a může dojít až k úplnému znecitlivění končetin. Citlivost se snižuje výhradně na končetinách, zejména pánevních a nejvíce v distálních částech. Směrem nahoru bývá postižení méně patrné. K rozvoji choroby dochází ve věku od 2. do 12. měsíce, nejčastěji ve 4. měsíci života. Onemocnění je autosomálně recesivní (k jeho vzniku je potřeba zdědění mutace od obou rodičů, kteří mohou být skrytí přenašeči). 5
Klinické příznaky a diagnostika
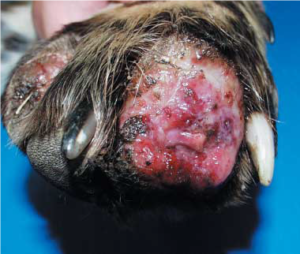
Nejvýznamnějším pozorovatelným příznakem je lízání až kousání tlapek. Tomuto jevu se odborně říká automutilace neboli sebemrzačení, sebepoškozování. To může probíhat jenom na jedné, více nebo i všech končetinách. Automutilace může dospět do takového stádia, že si psi doslova „uhryžou prsty“. Mutilace predisponuje ke vzniku pododermatitidy (zánět kůže nohy), paronychie (zánět drápového lůžka) až osteomyelitidy (zánět kostní tkáně) po proniknutí bakterií kontaminujících rány do hloubky. Na kůži tlapek a polštářcích mohou vzniknout nehojící se vředy a hypergranulační tkáň. Cytologií bývají z těchto lézí prokázány neutrofilní a eosinofilní granulocyty a makrofágy, tedy bílé krvinky, jako buněčná složka imunitního systému a různé druhy bakterií.
Při klinickém vyšetření bývá zjišťována necitlivost distálních částí končetin na bolest, jež se nejčastěji testuje sevřením kůže peanem. Tento příznak je často obtížně hodnotitelný, protože zde může hrát roli individuální práh bolesti a psa se jednoduše nemůžeme zeptat, co cítí, nebo necítí, tak jako tomu je u lidských pacientů. I z toho důvodu tento příznak většinou chovatelé vůbec nezaregistrují. Ve vývoji nemoci však hraje podstatnou roli. Díky tomu, že zvíře necítí bolest, dochází častěji k různým mikrofrakturám kostí či vymknutí kloubů a pravděpodobně až následně k lízaní postižené končetiny. Jedinci trpící tímto syndromem jsou schopni normálního pohybu i přes velmi výrazná poranění, nedochází ke kulhání, či ataxii (nekoordinovaným pohybům). Při vyšetření jsou také vyvolatelné všechny končetinové míšní poklepové reflexy a normální propriorecepce. To koresponduje s výše zmíněným tvrzením, že postižena jsou pouze senzorická nervová vlákna, tedy taková, která přenáší vjemy z periferie do centrální nervové soustavy.
Definitivní diagnóza tohoto onemocnění je založena na vyloučení všech ostatních příčin automutilace, zejména potravinových alergií, ektoparazitóz, přítomnosti cizího tělesa, atopické dermatitidy a dalších či podobné nemoci zvané „acral lick dermatitis“, jež se projevuje také sebepoškozováním, ale nesouvisí s nervovým poškozením, nýbrž se jedná o psychologickou poruchu. Podmínkou správně diagnózy je dobrá anamnéza včetně rodokmenu, klinické příznaky, především analgezie (necitlivost na bolestivé podněty) a v neposlední řadě také postmortální vyšetření. Makroskopické a histopatologické nálezy jsou typické: menší velikost míšních ganglií, redukce celkového počtu neuronů v těchto gangliích, změna poměru velkých a malých neuronů ve prospěch malých a redukce vláken v dorsolaterálním svazku míchy. V dnešní době je díky relativně nové studii, která identifikovala genetickou podstatu choroby, možnost testovat rodičovské páry pro vhodnost k plemenitbě. 1,2,3,5,6,7
Terapie
Žádná specifická terapie bohužel neexistuje, a proto je zapotřebí nemoci předcházet krytím pouze jedinců se známým genotypem. Management již rozvinuté choroby je časově, finančně i psychicky náročný. Jediné, co můžeme pro zkvalitnění života udělat, je ošetřování ran, bandážování a zamezení mutilace pomocí krčních ochranných límců nebo náhubků. V krajních případech je možné přistoupit k amputaci postižené končetiny. Ačkoliv byly popsány případy, kdy se psi dožili dospělosti a příznaky onemocnění vymizely, většinou se majitelé rozhodnou pro eutanazii postižených jedinců, protože již nadále nezvládají vyčerpávající péči.2,5
Význam
AMS a výzkum s ním spojený slouží jako model pro podobné onemocnění u lidí, zvané Charcot-Marie-Toothova choroba. Nedávná lokalizace mutace by mohla do budoucna pomoci ve vývoji genetické léčby.5
Reference:
- Cummings JF, de Lahunta A, Winn SS. Acral mutilation and nociceptive loss in English Pointer dogs. Acta Neuropathol. 1981;53(2):119-127. doi:10.1007/BF00689992
- PARADIS M, JAHAM CDE, PAGE N, SAUVE F, HELIE P. Acral mutilation and analgesia in 13 French spaniels. Vet Dermatol. 2005;16(2):87-93.
- Bardagí M, Montoliu P, Ferrer L, Fondevila D, Pumarola M. Acral Mutilation Syndrome in a Miniature Pinscher. J Comp Pathol. 2011;144(2):235-238. doi:https://doi.org/10.1016/j.jcpa.2010.08.014
- Granger N. Canine inherited motor and sensory neuropathies: An updated classification in 22 breeds and comparison to Charcot–Marie–Tooth disease. Vet J. 2011;188(3):274-285. doi:https://doi.org/10.1016/j.tvjl.2010.06.003
- Plassais J, Lagoutte L, Correard S, et al. A Point Mutation in a lincRNA Upstream of GDNF Is Associated to a Canine Insensitivity to Pain: A Spontaneous Model for Human Sensory Neuropathies. PLOS Genet. 2016;12(12):e1006482. https://doi.org/10.1371/journal.pgen.1006482.
- Cummings JF, de Lahunta A, Braund KG, Mitchell Jr WJ. Hereditary sensory neuropathy. Nociceptive loss and acral mutilation in pointer dogs: canine hereditary sensory neuropathy. Am J Pathol. 1983;112(1):136-138. https://www.ncbi.nlm.nih.gov/pubmed/6574711.
- Wynchank D, Berk M. Fluoxetine treatment of acral lick dermatitis in dogs: A placebo-controlled randomized double blind trial. Depress Anxiety. 1998;8(1):21-23. doi:10.1002/(SICI)1520-6394(1998)8:1<21::AID-DA4>3.0.CO;2-8
- Syndrom akrální mutilace - 22 srpna, 2019
- Juvenilní myoklonická epilepsie u rhodéských ridgebacků - 2 srpna, 2019




Buďte první kdo přidá komentář